核心突破:雙臨床試驗獲批揭示技術成熟度躍遷
近日,國家藥品監督管理局接連批準兩款臍帶間充質干細胞(MSC)注射液開展2型糖尿病臨床試驗,標志著干細胞治療從基礎研究向臨床轉化邁出關鍵一步。其中,HF001注射液作為國家1類新藥率先進入臨床階段,聚焦于通過調節免疫微環境修復胰島功能;而此前獲批的E10I注射液已于8月啟動多中心患者招募。兩者的差異化布局與快速推進,既凸顯了監管部門對創新療法的審慎支持,也印證了干細胞技術在代謝性疾病領域的巨大潛力。

為何選擇干細胞?——從"治標"到"治本"的范式革新
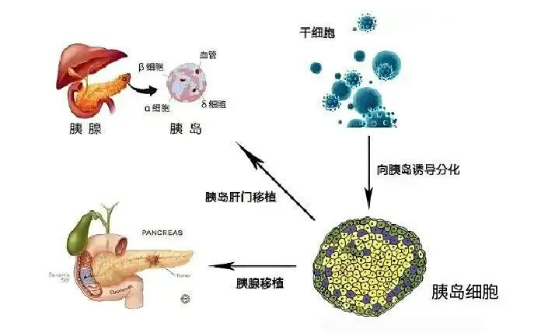
傳統降糖治療多依賴外源性藥物干預,而干細胞療法通過以下機制實現"修復式控糖":
微環境重塑:抑制慢性炎癥反應,改善胰島β細胞生存土壤;
功能激活:分泌生長因子促進血管新生及組織修復;
系統調節:增強機體對胰島素的敏感性,重建代謝平衡。
正如301醫院開展的隨機對照研究所示,接受干細胞輸注的患者不僅血糖波動幅度降低37%,且C肽水平(反映胰島功能的關鍵指標)顯著回升,印證了其標本兼治的獨特優勢。
臨床試驗分層推進:從單中心驗證到多區域協同
301醫院的高質量循證實踐:歷時三年的對照試驗數據顯示,干細胞治療組HbA1c達標率提升42%,低血糖事件發生率下降61%,為后續大規模應用提供了安全性與有效性基準。
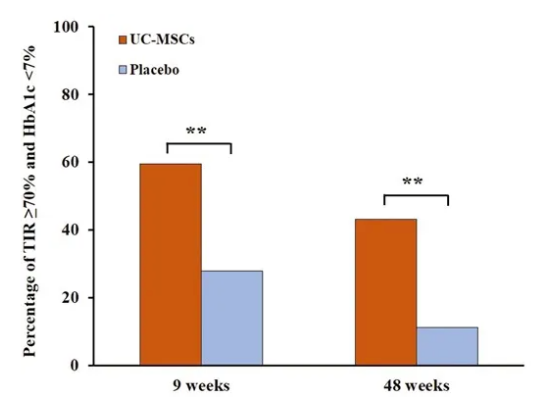
中山一院牽頭的多中心突破:聯合多家三甲醫院開展的靜脈輸注研究,通過標準化操作流程擴大樣本量,重點探索不同病程患者的最佳干預時機。這種協作模式不僅加速數據積累,更為療法的普適性驗證奠定基礎。

政策信號解析:從科研突破到產業落地的制度保障
國家藥監部門在短期內密集批準同類療法臨床試驗,釋放出三重積極信號:
技術認可:MSC療法通過嚴謹的臨床前評價與早期試驗,獲得官方背書;
路徑打通:建立針對細胞治療產品的快速審評通道,加速產學研轉化;
需求導向:針對糖尿病防控嚴峻形勢,鼓勵開發根治性解決方案。
此舉預示著我國再生醫學領域進入"制度創新+技術創新"雙輪驅動的新周期。
未來展望:從實驗室到病床的跨越式發展
隨著兩項臨床試驗的深入推進,干細胞治療有望破解當前糖尿病管理的三大痛點:
并發癥防控:通過修復血管內皮損傷,降低腎病、視網膜病變等并發風險;
個體化醫療:基于患者免疫狀態定制細胞治療方案;
長期獲益:相較于終身服藥,實現胰島功能的可持續恢復。
行業領軍企業已開始布局全產業鏈,從細胞制備工藝優化到AI輔助療效預測,技術創新與臨床需求的深度融合將重構糖尿病治療格局。對于廣大患者而言,"修復式控糖"時代的曙光已現。
免責聲明:
文章僅用于科普交流,無任何商業目的不作任何商業用途,亦不表示任何醫療聲明或建議。我們尊重原創,也注重分享。圖文來源網絡,版權歸原作者所有,如涉及作品內容、版權或其它問題,請聯系我們刪除!


 閩公網安備 35020602002648 號
閩公網安備 35020602002648 號 QQ 客服
QQ 客服
